ΑΝΤΙΚΕΙΜΕΝΟ ΚΑΙ ΣΤΟΧΟΙ ΤΟΥ ΕΡΓΟΥ
H Έρευνα & Καινοτομία ιδιαίτερα στον τομέα των φαρμάκων αποτελεί μία από τις πρώτες, στρατηγικής σημασίας προτεραιότητες παγκοσμίως γιατί είναι ζωτικής σημασίας για την υγεία και τη βελτίωση της ποιότητας ζωής των ασθενών, οι οποίοι πρέπει να έχουν πρόσβαση σε ασφαλή, καινοτόμα και προσιτά φάρμακα.
Αντικείμενο του έργου Πειραματικής Ανάπτυξης LFOS4Glaucoma είναι η ανάπτυξη ενός καινοτόμου οφθαλμικού διαλύματος λατανοπρόστης χωρίς συντηρητικά (για τη βελτίωση της υπάρχουσας φαρμακοτεχνικής μορφής XALATAN®) που θα συσκευαστεί στον περιέκτη Novelia®PFS για την ελάττωση της αυξημένης ενδοφθάλμιας πίεσης σε οφθαλμική υπερτονία και γλαύκωμα ανοιχτής γωνίας με στόχο να συμβάλλει στην χρόνια κλινική αντιμετώπιση ασθενειών με χαμηλή συμμόρφωση ασθενών.
Το έργο αποτελεί Αξιοποίηση Ερευνητικών Αποτελεσμάτων της εταιρείας RAFARM γιατί η ανάπτυξη του οφθαλμικού διαλύματος λατανοπρόστης χωρίς συντηρητικά θα βασιστεί στην μέθοδο παρασκευής οφθαλμικών φαρμακευτικών συνθέσεων πολλαπλών δόσεων για τοπική χορήγηση, απουσία αντιμικροβιακών συντηρητικών για την οποία η εταιρεία έχει ήδη κατοχυρώσει δίπλωμα ευρεσιτεχνίας (GR20130100709, ημ/νία δημοσίευσης: 12/05/2015). Συγκεκριμένα, η εφεύρεση αναφέρεται σε μια οφθαλμική φαρμακευτική σύνθεση (ελεύθερη συντηρητικού) για τοπική χορήγηση η οποία περιλαμβάνει μια θεραπευτικά αποτελεσματική ποσότητα δραστικής ουσίας (ανάλογο προσταγλανδίνης ή φθοροκινολόνη ή αναστολέα της καρβονικής αντίδρασης ή ανταγωνιστή β-αδρενεργητικού υποδοχέα) και στην μέθοδο παραγωγής της. Σκοπός της εταιρείας είναι η ανάπτυξη ενός υπεργενόσημου προϊόντος λατανοπρόστης (μέχρι σήμερα δεν κυκλοφορεί αντίστοιχο προϊόν στην Ευρώπη) με την βελτίωση της υπάρχουσας φαρμακοτεχνικής μορφής XALATAN®.
Το γλαύκωμα είναι μια ομάδα νόσων του οφθαλμού που χαρακτηρίζεται από βλάβη στο οπτικό νεύρο και αποτελεί την κύρια αιτία μη αναστρέψιμης τύφλωσης σε παγκόσμιο επίπεδο. Εκτιμάται ότι το 2010 64,3 εκατομμύρια άτομα παγκοσμίως επηρεάστηκαν από πρωτοπαθές γλαύκωμα ανοικτής και κλειστής γωνίας. Λόγω της ταχείας αύξησης του γηριατρικού πληθυσμού παγκοσμίως, ο αριθμός αυτός προβλέπεται να αυξηθεί περαιτέρω σε 76 εκατομμύρια το 2020 και 111,8 εκατομμύρια το 2040.
Ο επιπολασμός του γλαυκώματος έχει σημαντικό άμεσο και έμμεσο κόστος υγειονομικής περίθαλψης (φαρμακευτικές αγωγές μείωσης ενδοφθάλμιας πίεσης, επισκέψεις σε γιατρούς και νοσοκομεία, νοσηλευτική φροντίδα στο σπίτι, μεταφορά, σκύλοι οδηγοί, απώλεια παραγωγικότητας, ημέρες που χάθηκαν από την εργασία κ.λπ) ακόμη και στα πρώτα στάδια της νόσου. Με την επιδείνωση της σοβαρότητας της νόσου, αυξάνονται οι απαιτήσεις υγειονομικής περίθαλψης. Σύμφωνα με μια ευρωπαϊκή μελέτη, το άμεσο κόστος θεραπείας αυξήθηκε κατά περίπου €86 για κάθε στάδιο του γλαυκώματος. Το ετήσιο κόστος κυμαίνεται από 455 ευρώ ανά άτομο (στάδιο 0) έως σε 969 ευρώ ανά άτομο το έτος (στάδιο 4). Με βάση τα ευρήματα αυτά, η αντιμετώπιση του γλαυκώματος και η αποτελεσματική καθυστέρηση της εξέλιξης της νόσου αναμένεται να μειώσει το οικονομικό βάρος της συγκεκριμένης ασθένειας
Το γλαύκωμα είναι μια εξουθενωτική ασθένεια για όσους νοσούν, με σημαντικό αντίκτυπο στην ποιότητα ζωής. Το ψυχολογικό φορτίο αυξάνεται όσο μειώνεται η όραση, υπάρχει αυξανόμενος φόβος τύφλωσης, κοινωνική απόσυρση από την μείωση της όρασης και κατάθλιψη. Οι κύριοι παράγοντες κινδύνου για την εμφάνιση γλαυκώματος περιλαμβάνουν την αυξημένη ενδοφθάλμια πίεση (IOP), τη μεγάλη ηλικία και το οικογενειακό ιστορικό γλαυκώματος.
Παρόλο που σε ασθενείς με γλαύκωμα παρατηρείται συχνά αυξημένη ενδοφθάλμια πίεση, ορισμένοι ασθενείς μπορεί να αναπτύξουν γλαυκωματική οπτική νευροπάθεια χωρίς τεκμηριωμένη υψηλή ενδοφθάλμια πίεση. Η οφθαλμική υπέρταση είναι μια πολύ πιο κοινή πάθηση από το γλαύκωμα. Πολλές μεγάλες, προοπτικές, πολυκεντρικές κλινικές δοκιμές έχουν αποδείξει όφελος από τη μείωση της ενδοφθάλμιας λειτουργίας στη θεραπεία του γλαυκώματος. Μελέτη θεραπείας της οφθαλμικής υπέρτασης (OHTS – Ocular hypertension treatment study) έδειξε ότι μείωση της ενδοφθάλμιας πίεσης κατά ≥20% με ιατρική θεραπεία μπορεί να μειώσει τον σχετικό κίνδυνο πρόκλησης στο γλαύκωμα κατά ~ 50% σε άτομα με οφθαλμική υπέρταση.
Πέντε κύριες κατηγορίες φαρμάκων για το γλαύκωμα είναι προς το παρόν διαθέσιμες για κλινική χρήση: α-αδρενεργικοί αγωνιστές (βριμονιδίνη), β-αδρενεργικοί ανταγωνιστές (β-αναστολείς, π.χ. τιμολόλη), αναστολείς της καρβονικής ανυδράσης (π.χ. βρινζολαμίδη, δορζολαμίδη), ανάλογα της προσταγλανδίνης (π.χ. λατανοπρόστη, τραβοπρόστη, βιματοπρόστη). Παρόλο που οι β-αναστολείς έχουν σημειώσει μεγάλη επιτυχία ως θεραπεία πρώτης γραμμής για το γλαύκωμα για πολλά χρόνια, πρόσφατα τα ανάλογα της προσταγλανδίνης έχουν κερδίσει έδαφος ως επιλογή πρώτης γραμμής για την αρχική θεραπεία ασθενών με γλαύκωμα ή οφθαλμική υπέρταση.
Τα φάρμακα κατά του γλαυκώματος μπορούν να μειώσουν την ενδοφθάλμια πίεση είτε μειώνοντας την παραγωγή υδατικού υγρού και/ή αυξάνοντας την εκροή του υδατικού υγρού. Η μονοθεραπεία προσφέρει σαφή πλεονεκτήματα στη θεραπεία του γλαυκώματος καθώς οι ασθενείς είναι πιθανότερο να μην συμμορφώνονται με τη θεραπεία όσο αυξάνει η πολυπλοκότητα του θεραπευτικού τους σχήματος. Ωστόσο, ένας συμπληρωματικός παράγοντας με συμπληρωματικό μηχανισμό δράσης στο φάρμακο πρώτης γραμμής μπορεί να προσφέρει μεγαλύτερη και πιο συνεπή μείωση της ενδοφθάλμιας πίεσης. Πρόσφατες μελέτες έχουν δείξει ότι α-αγωνιστές, β-αναστολείς και αναστολείς της καρβονικής ανυδράσης μπορούν να χρησιμοποιηθούν με ασφάλεια και αποτελεσματικά σε συνδυασμό με ανάλογα της προσταγλανδίνης.
Το σκεύασμα που θα επιλεγεί για τη θεραπεία του γλαυκώματος θα πρέπει να παρέχει εξαιρετική αποτελεσματικότητα στην μείωση της ενδοφθάλμιας πίεσης με τις ελάχιστες δυνατές ανεπιθύμητες ενέργειες. Η αποτελεσματικότητα της θεραπείας σε ασθενείς με γλαύκωμα /οφθαλμική υπέρταση καθορίζεται σε μεγάλο βαθμό από το μακροπρόθεσμο προφίλ ανοχής του φαρμάκου, το οποίο με τη σειρά του εξαρτάται από τα ειδικά με τη σύνθεση χαρακτηριστικά. Οι πιο κοινές φαρμακοτεχνικές μορφές των οφθαλμικών σκευασμάτων είναι τα διαλύματα (62,4%), οι αλοιφές (17,4%) και τα εναιωρήματα (8,7%). Τα παραπάνω αντιπροσωπεύουν σχεδόν το 90% των διαθέσιμων σήμερα οφθαλμικών σκευασμάτων. Τα οφθαλμικά διαλύματα, αποτελούν πρώτη προτεραιότητα για τους παραγωγούς, δεδομένου ότι είναι σχετικά απλά στην παρασκευή, διήθηση και αποστείρωση.
Από τα οφθαλμικά διαλύματα που χρησιμοποιούνται συχνότερα για τη θεραπεία του πρωτογενούς γλαυκώματος ανοιχτής γωνίας και της οφθαλμικής υπέρτασης, η λατανοπρόστη ενδείκνυται για την μείωση της αυξημένης ενδοφθάλμιας πίεσης σε ενήλικους ασθενείς με γλαύκωμα ανοιχτής γωνίας και οφθαλμική υπερτονία και σε παιδιατρικούς ασθενείς με αυξημένη ενδοφθάλμια πίεση και παιδιατρικό γλαύκωμα.
Φαρμακολογικά, η λατανοπρόστη, ανάλογο της προσταγλανδίνης F2α, είναι εκλεκτικός αγωνιστής υποδοχέων prostanoid FP που μειώνει την ενδοφθάλμια πίεση αυξάνοντας την εκροή του υδατοειδούς υγρού. Η μείωση της ενδοφθάλμιας πίεσης στον άνθρωπο αρχίζει περίπου τρεις μέχρι τέσσερις ώρες μετά τη χορήγηση και το μέγιστο αποτέλεσμα επιτυγχάνεται μετά από 8-12 ώρες. Παρά την εξαιρετική συστηματική ασφάλεια της λατανοπρόστης, μπορεί να παρατηρηθούν τοπικές ανεπιθύμητες παρενέργειες που προκαλούνται από την δραστική ουσία και από το χλωριούχο βενζαλκόνιο που χρησιμοποιείται ως συντηρητικό στο εγκεκριμένο οφθαλμικό σκεύασμα Xalatan (0.005% οφθαλμικό διάλυμα που περιέχει 0.02% χλωριούχο βενζαλκόνιο). Τοπικές ανεπιθύμητες ενέργειες περιλαμβάνουν μεταβολές στην οφθαλμική επιφάνεια προκαλώντας φλεγμονή και δυσλειτουργία του επιθηλίου του επιπεφυκότος και οδηγώντας σε διάφορες άλλες οφθαλμολογικές διαταραχές συμπεριλαμβανομένης της ξηροφθαλμίας (DED), της διόγκωσης του επιπεφυκότος και της βλεφαρίτιδας. Η χρόνια έκθεση στο ΒΑΚ προκαλεί έμμεσες και άμεσες τοξικές επιδράσεις στην οφθαλμική επιφάνεια με μειωμένη κυτταρική βιωσιμότητα και μειωμένη λειτουργία επιθηλιακού φραγμού. Ως αποτέλεσμα, η δυσφορία και η δυσαρέσκεια των ασθενών μπορεί να οδηγήσουν σε κακή συμμόρφωση με τη θεραπεία, αποτυχία θεραπείας και τελικά σε εξέλιξη της νόσου.
Το 2011, εγκρίθηκε το πρώτο σκεύασμα λατανοπρόστης χωρίς συντηρητικά Monoprost® (Laboratoires Théa, ClermontFerrand, Γαλλία) Κλινικές μελέτες φάσης ΙΙ και φάσης ΙΙΙ έδειξαν ότι η λατανοπρόστη χωρίς συντηρητικά έχει παρόμοια αποτελεσματικότητα ενώ είναι καλύτερα ανεκτή σε σύγκριση με το οφθαλμικό σκεύασμα της λατανοπρόστης που περιέχει συντηρητικά. Το καλύτερο προφίλ οφθαλμικής ανοχής της λατανοπρόστης χωρίς συντηρητικά επιβεβαιώθηκε μέσω της χαμηλότερης επίπτωσης τοπικών ανεπιθύμητων ενεργειών και της υπεραιμίας του επιφεφυκότα σε σύγκριση με τις οφθαλμικές σταγόνες που περιέχουν συντηρητικά. Με βάση τα παραπάνω ο Ευρωπαϊκός Οργανισμός Φαρμάκων (EMA) αναγνώρισε την ανάγκη για οφθαλμικά σκευάσματα χωρίς συντηρητικά για τους ασθενείς που δεν ανέχονται οφθαλμικές σταγόνες με συντηρητικά, οι οποίοι χρειάζονται χρόνιες χορηγήσεις οφθαλμικών σταγόνων καθώς και για παιδιατρικούς ασθενείς, ιδιαίτερα για τα νεογνά. Ο EMA σαφώς ενθάρρυνε τις φαρμακευτικές εταιρείες να αναπτύξουν οφθαλμικές σταγόνες χωρίς συντηρητικά, όποτε αυτό είναι εφικτό.
Το εγκεκριμένο σκεύασμα της λατανοπρόστης χωρίς συντηρητικά, Monoprost, είναι συσκευασμένο σε περιέκτη μονής δόσης. Ωστόσο, μεγάλος αριθμός ασθενών που λαμβάνουν λατανοπρόστη είναι ηλικιωμένοι ασθενείς που λόγω της μειωμένης επιδεξιότητας και της όρασης έχουν σημαντική δυσκολία στο χειρισμό οφθαλμικών περιεκτών μονής δόσης. Για να αντιμετωπιστούν οι ανάγκες αυτών των ασθενών, έχουν αναπτυχθεί διάφοροι οφθαλμολογικοί περιέκτες πολλαπλών δόσεων που εμποδίζουν την μικροβιακή μόλυνση αφότου ανοιχτούν.
Στα πλαίσια του έργου το προς ανάπτυξη οφθαλμικό διάλυμα λατανοπρόστης, ελεύθερο συντηρητικού βασισμένο πάνω στην οφθαλμική φαρμακευτική σύνθεση και την μέθοδο παρασκευής της εφεύρεσης της εταιρείας RAFARM θα συσκευαστεί στον περιέκτη Novelia®PFS με στόχο ο συνδυασμός φαρμακοτεχνικής μορφής και συσκευής να επιτυγχάνει μια ΣΤΟχευμένη θεραπεία για την ελάττωση της αυξημένης ενδοφθάλμιας πίεσης σε οφθαλμική υπερτονία και γλαύκωμα ανοιχτής γωνίας
Η συσκευή Novelia®PFS έχει σχεδιαστεί με βαλβίδα μονής κατεύθυνσης και βύσμα σιλικόνης που λειτουργεί ως σύστημα εξαερισμού, το οποίο επιτρέπει μεν την είσοδο αέρα στον περιέκτη κατά τη χρήση, αλλά εμποδίζει παράλληλα την είσοδο μικροβίων στο μπουκάλι και τη μόλυνση των περιεχομένων. Επιπλέον, για να αποφευχθεί η επιμόλυνση λόγω πτώσης της υπολειπόμενης σταγόνας, το καπάκι και το τμήμα που περιβάλλει το ακροστόμιο της συσκευής περιέχουν άργυρο ως αντιμικροβιακό παράγοντα. Ωστόσο, δεν υπάρχει άμεση επαφή μεταξύ του φαρμακευτικού προϊόντος και των μερών που περιέχουν άργυρο, καθώς ο αντιμικροβιακός παράγοντας εντοπίζεται μόνο στα ως άνω μέρη της συσκευής.
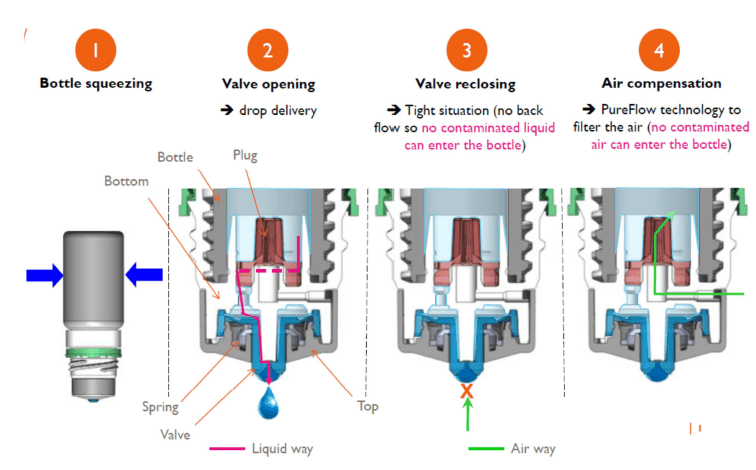
Μηχανισμός λειτουργίας της συσκευής Novelia®PFS
Σε συμφωνία με τις συστάσεις του ΕΜΑ, στόχος του έργου είναι η ανάπτυξη ενός καινοτόμου οφθαλμικού διαλύματος λατανοπρόστης χωρίς συντηρητικά (για τη βελτίωση της υπάρχουσας φαρμακοτεχνικής μορφής XALATAN®) που θα συσκευαστεί στον περιέκτη Novelia®PFS. Το αποτέλεσμα του έργου, διάρκειας 24 μηνών, είναι ένα έτοιμο προς έγκριση υπέρ-γενόσημο προϊόν, η ανάπτυξη και η παραγωγή του οποίου συμμορφώνεται με τους κανόνες Ορθής Παρασκευστικής Πρακτικής (cGMPs). Η εταιρεία στην συνέχεια του προγράμματος θα μπορεί να ολοκληρώσει το πρόγραμμα κλινικών μελετών σύμφωνα με τους κανονισμούς της ΕΕ έτσι ώστε να συγκεντρωθούν όλα τα απαραίτητα δεδομένα για την υποβολή φακέλου, ενώ το καινοτόμο προϊόν που θα κατοχυρωθεί με δίπλωμα ευρεσιτεχνίας και επέκταση της υπάρχουσας πατέντας της εταιρείας θα συμβάλει στην ανάπτυξη και την εξωστρέφεια της εταιρείας και ως εκ τούτου θα ενισχύσει την ανταγωνιστικότητα της ελληνικής οικονομίας.
Το υπεργενόσημο σκεύασμα (value added medicine) οφθαλμικού διαλύματος Λατανοπρόστης πολλαπλών δόσεων, ελεύθερο συντηρητικού, σε περιέκτη Novelia®PFS στοχεύει την υψηλή ικανοποίηση των ασθενών όσον αφορά την ανοχή στην έναρξη της θεραπείας που είναι το κλειδί για ένα επιτυχές, συνεχές και σταθερό θεραπευτικό όφελος στο γλαύκωμα. Το πρόγραμμα Ε&Α LFOS4Glaucoma βασίζεται στους παρακάτω άξονες-ενέργειες:
- την προ-μορφοποίηση του προϊόντος (Preformulation)
- τον σχεδιασμό ανάπτυξης σύμφωνα με τη μεθοδολογία Quality by Design (QbD)
- την κυρίως ανάπτυξη (Core Development)
- την παραγωγή πιλοτικών παρτίδων και την επικύρωση της παραγωγικής διαδικασίας
- τις μελέτες σταθερότητας του προϊόντος
- τον σχεδιασμό του προκλινικού και κλινικού προγράμματος (Scientific advice)
Tα αποτελέσματα του ερευνητικού έργου LFOS4Glaucoma με την ανάπτυξη ενός καινοτόμου διαλύματος Λατανοπρόστης πολλαπλών δόσεων ελεύθερο συντηρητικού σε περιέκτη Novelia®PFS το οποίο αναπτύχθηκε για πρώτη φορά στην Ελλάδα και δεν είναι διαθέσιμο στην Ευρωπαϊκή Ένωση είναι:
- η βελτιωμένη διαλυτότητα και υψηλή σταθερότητα έναντι αντιστοίχων οφθαλμικών σκευασμάτων που παρέχονται υπό την μορφή διαλυμάτων
- η βελτιωμένη ανεκτικότητα από τον ασθενή, λόγω απουσίας συντηρητικού
- η αύξηση της συμμόρφωσης του ασθενούς
- η συμβολή στην χρόνια κλινική αντιμετώπιση ασθενειών με χαμηλή συμμόρφωση ασθενών
- η βελτίωση της αποτελεσματικότητας της θεραπείας
- η σταθεροποίηση της απόκρισης του ασθενούς στην θεραπεία
- η μεγαλύτερη ασφάλεια από την χορήγηση φαρμάκων
- το μειωμένο κόστος για το φορέα περίθαλψης και για τον ίδιο τον ασθενή αφού το κόστος θεραπείας με περιέκτες μονής δόσης είναι πολύ μεγαλύτερο
Το έργο LFOS4Glaucoma, είναι άρρηκτα συνδεμένο με τις επιχειρηματικές και επιχειρησιακές στρατηγικές του κλάδου και καθορίζεται με βάση τις τεχνολογικές εξελίξεις, τα ευρήματα της Έξυπνης Ειδίκευσης (RIS3) και την αξιοποίηση των συγκριτικών εγχώριων πλεονεκτημάτων. Το έργο αποτελεί Αξιοποίηση Ερευνητικών Αποτελεσμάτων της εταιρείας RAFARM, και εντάσσεται στην κατηγορία Έρευνας στον τομέα των Φαρμακευτικών προϊόντων διότι αφορά την ανάπτυξη νέων φαρμακευτικών μορφών προστιθέμενης αξίας και δυνατότητας εξαγωγής (μέχρι σήμερα δεν κυκλοφορεί αντίστοιχο προϊόν στην Ευρώπη) βασισμένη σε ήδη υπάρχουσα πατέντα της εταιρείας που σε συνδυασμό με εξειδικευμένη συσκευή επιτυγχάνουν επιτυχή ΣΤΟχευμένη χορήγηση του φαρμάκου για την ελάττωση της αυξημένης ενδοφθάλμιας πίεσης σε οφθαλμική υπερτονία και γλαύκωμα ανοιχτής γωνίας.
Αναφορές
[1] Tham YC, Li X, Wong TY, Quigley HA, Aung T, Cheng CY. Global prevalence of glaucoma and projections of glaucoma burden through 2040: a systematic review and meta-analysis. Ophthalmology. 2014 Nov;121(11):2081-90.
[2] Varma R, Lee PP, Goldberg I, Kotak S. An assessment of the health and economic burdens of glaucoma. Am J Ophthalmol. 2011 Oct;152(4):515-22.
[3] Traverso CE, Walt JG, Kelly SP, Hommer AH, Bron AM, Denis P, Nordmann JP, Renard JP, Bayer A, Grehn F, Pfeiffer N, Cedrone C, Gandolfi S, Orzalesi N, Nucci C, Rossetti L, Azuara-Blanco A, Bagnis A, Hitchings R, Salmon JF, Bricola G, Buchholz PM, Kotak SV, Katz LM, Siegartel LR, Doyle JJ. Direct costs of glaucoma and severity of the disease: a multinational long term study of resource utilisation in Europe. Br J Ophthalmol. 2005 Oct;89(10):1245-9.
[4] Coleman AL, Kodjebacheva G. Risk factors for glaucoma needing more attention. Open Ophthalmol J. 2009 Sep 17;3:38-42.
[5] Kass MA, Heuer DK, Higginbotham EJ, Johnson CA, Keltner JL, Miller JP, Parrish RK 2nd, Wilson MR, Gordon MO. The Ocular Hypertension Treatment Study: a randomized trial determines that topical ocular hypotensive medication delays or prevents the onset of primary open-angle glaucoma. Arch Ophthalmol. 2002 Jun;120(6):701-13; discussion 829-30.
[6] Conlon R, Saheb H, Ahmed II. Glaucoma treatment trends: a review. Can J Ophthalmol. 2017 Feb;52(1):114-124.
[7] Saettone et al. Ophthalmic emulsions and suspensions. Journal of Toxicology: Cutaneous and Ocular toxicology. 2001, Volume 20: Issue 2-3, pages 183-201.
[8] Summary of Product Characteristics Xalatan 50 micrograms/ml eye drops solution https://www.medicines.org.uk/emc/product/1616/smpc
[9] Baudouin C, Labbé A, Liang H, Pauly A, Brignole-Baudouin F. Preservatives in eyedrops: the good, the bad and the ugly. Prog Retin Eye Res. 2010;29(4):312–334.
[10] Jaenen N, Baudouin C, Pouliquen P, Manni G, Figueiredo A, Zeyen T. Ocular symptoms and signs with preserved and preservative-free glaucoma medications. Eur J Ophthalmol. 2007;17(3):341–349.
[11] Rouland JF, Traverso CE, Stalmans I, et al; T2345 Study Group. Efficacy and safety of preservative-free latanoprost eyedrops, compared with BAK-preserved latanoprost in patients with ocular hypertension or glaucoma. Br J Ophthalmol. 2013;97(2):196–200.
[12] Summary of product characteristics MONOPOST latanoprost 50 mcg/ml eye drops, solution in single-dose container https://www.medicines.org.uk/emc/product/2978/smpc
[13] Rouland JF, Traverso CE, Stalmans I, et al; T2345 Study Group. Efficacy and safety of preservative-free latanoprost eyedrops, compared with BAK-preserved latanoprost in patients with ocular hypertension or glaucoma. Br J Ophthalmol. 2013;97(2):196–200.
[14] Aptel F, Choudhry R, Stalmans I. Preservative-free versus preserved latanoprost eye drops in patients with open-angle glaucoma or ocular hypertension. Curr Med Res Opin. 2016;32(8):1457–1463.
[15] Cucherat M, Stalmans I, Rouland JF. Relative efficacy and safety of preservative-free latanoprost (T2345) for the treatment of open-angle glaucoma and ocular hypertension: an adjusted indirect comparison meta-analysis of randomized clinical trials. J Glaucoma. 2014;23(1):e69–e75.
[16] EMEA/622721/2009 EMEA PUBLIC STATEMENT ON ANTIMICROBIAL PRESERVATIVES IN OPHTHALMIC PREPARATIONS FOR HUMAN USE http://www.techtran.co.jp/ reportd/emea091208.pdf
[17] Novelia eye dropper https://www.nemera.net/products/ophthalmic-novelia-eyedropper/
